在醫療器械行業快速發展的今天,合規性是確保產品成功上市并持續運營的關鍵。中國作為全球重要的醫療器械市場,其法規體系日益完善且要求嚴格,企業需應對從產品注冊、生產質量管理到上市后監督的全周期監管。杭州瑞旭科技集團作為國內領先的技術咨詢服務機構,專注于為中國及國際醫療器械企業提供全面、專業的法規咨詢服務,助力企業高效應對合規挑戰,加速市場準入。
一、中國醫療器械法規環境概述
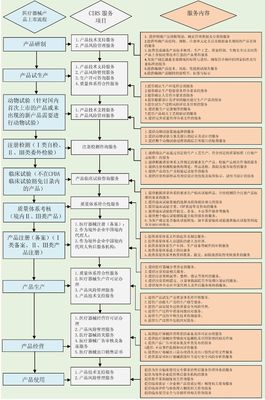
中國的醫療器械監管遵循《醫療器械監督管理條例》為核心的法律框架,由國家藥品監督管理局(NMPA)負責實施。根據風險等級,醫療器械分為一類、二類和三類,監管要求逐級提高。企業需完成產品備案或注冊、生產許可、臨床試驗(如適用)、質量體系核查等環節,流程復雜且耗時較長。NMPA持續推進法規與國際接軌,如加入國際醫療器械監管機構論壇(IMDRF),但本土化要求依然顯著,企業常面臨法規解讀不清晰、申請材料準備繁瑣等難題。
二、杭州瑞旭科技集團的核心服務領域
杭州瑞旭科技集團憑借多年行業經驗,構建了覆蓋醫療器械全生命周期的咨詢服務體系,主要包括:
- 產品注冊與備案支持:針對不同類別醫療器械,提供從分類界定、注冊路徑規劃到申報資料編寫的全程輔導。團隊熟悉NMPA最新指南,能幫助企業優化技術文件,提高注冊成功率。例如,對于創新醫療器械,瑞旭可協助申請綠色通道,縮短審批時間。
- 質量管理體系合規:依據《醫療器械生產質量管理規范》(GMP)要求,為企業建立或優化質量體系,包括文件管理、生產過程控制、供應商審核等。瑞旭提供培訓和現場指導,確保企業通過NMPA的體系核查,并持續符合ISO 13485等國際標準。
- 臨床試驗設計與監督:對于需臨床評價的二類、三類器械,瑞旭協助設計符合法規的試驗方案,管理臨床機構合作,并監督試驗過程,確保數據真實可靠,滿足注冊要求。
- 上市后監管與合規維護:產品上市后,企業需履行不良事件監測、召回管理等義務。瑞旭提供定期法規更新培訓、上市后研究支持,幫助企業應對NMPA的監督檢查,降低違規風險。
- 國際法規協調:針對出口企業,瑞旭提供歐美、東南亞等市場的法規咨詢,協助實現全球合規布局,例如CE認證、FDA注冊等,提升產品國際競爭力。
三、瑞旭科技的技術咨詢優勢
- 專業團隊:瑞旭匯聚了資深法規專家、技術工程師和臨床研究員,多數成員擁有NMPA或國際機構工作背景,能精準解讀政策動向。
- 本地化經驗:作為扎根杭州的機構,瑞旭深諳中國監管實踐,與地方藥監部門保持良好溝通,可為企業提供定制化解決方案。
- 數字化工具:利用信息化平臺,瑞旭為客戶提供法規數據庫查詢、流程跟蹤服務,提高咨詢效率,降低人為錯誤。
- 案例豐富:已成功協助數百家醫療器械企業完成產品注冊,涵蓋影像設備、體外診斷試劑、植入材料等多個領域,口碑良好。
四、企業合作價值與未來展望
選擇杭州瑞旭科技集團的咨詢服務,企業不僅能節省時間和成本,更可規避合規風險,專注于產品研發與市場拓展。隨著中國醫療器械法規持續演進(如人工智能器械、遠程醫療產品的新規出臺),瑞旭將持續更新服務內容,助力行業創新。建議企業在產品設計早期即介入法規咨詢,以“合規先行”策略贏取市場先機。
醫療器械的法規合規是一項系統工程,杭州瑞旭科技集團以技術為驅動,為企業搭建了可靠的合規橋梁。無論是初創公司還是跨國企業,都能從中獲得專業支持,實現在中國市場的穩健發展。